補助人工心臓(VAD)について
補助人工心臓(VAD)について
日本の補助人工心臓(VAD)治療は1980 年に三井記念病院で東大型補助人工心臓が使用されたことに始まっています。日本臨床補助人工心臓研究会の集計では、2013年8月までに1,627例が登録されています。
J-MACS *1)では平成22年(2010年)6月に患者登録を開始しました。平成26年(2014年)12月までの登録患者数424例であり、その推移は下記のとおりです。
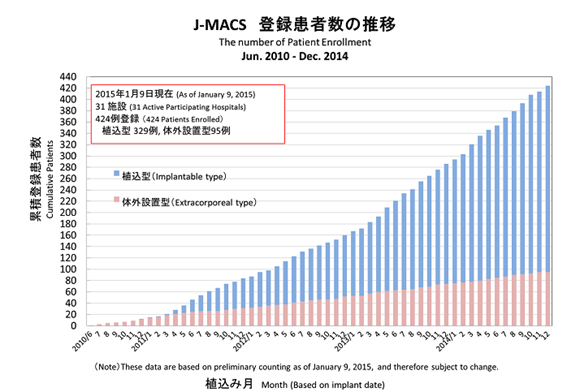
[出典]
「日本における補助人工心臓に関連した市販後のデータ収集(J-MACS:Japanese registry for Mechanically Assisted Circulatory Support)」
http://www.pmda.go.jp/safety/surveillance-analysis/0009.html
補助人工心臓(VAD)の役割
補助人工心臓(VAD)には大きく分けて下記の3つの役割があります。
- BTT(Bridge to Transplantation):心臓移植までの橋渡し
- BTR(Bridge to Recover):心臓の機能回復までの橋渡し
- DT(Destination Therapy):心不全治療としての恒久的使用
人工心臓の種類
人工心臓には完全置換型人工心臓(TAH)と補助人工心臓(VAD)があります。
TAHは自己の心臓を取り除き人工心臓に置換するものであり、循環は完全に人工心臓に依存します。
VADは自己の心臓を温存し、自己心機能と協調的に心拍出を補助します。VADは左心室の補助を行う左心室補助人工心臓(LVAD)、右心室の補助を行う右心室補助人工心臓(RVAD)、両心室の補助を行う両心室補助人工心臓(BVAD)に分類されます。
また、拍動流の有無により、拍動流型人工心臓と連続流型人工心臓(無拍動流型)に分かれます。拍動流型人工心臓は生体と同じような拍動流を生み出すシステムで、より生理的であるという長所がありますが、人工弁が必要であることや装置が大型化するという欠点があります。
一方、連続流型人工心臓は、脈のない流れを生み出すシステムで、人工弁が不要であることや小型化・耐久性等の点で利点がありますが、無拍動流という非生理的な循環が生体に及ぼす影響が懸念されます。現在臨床で使用されている人工心臓は、連続流型のLVADが大半となっています。
適応について
植込み型VADの選択基準と除外基準
植込み型VADの適応は、欧米ではBTTとDTの2つに分けられますが、日本ではBTTに限定されています。植込み型VADの患者選択基準と除外基準は「重症心不全に対する植込み型補助人工心臓治療ガイドライン」にて示されています。
植込み型VADの実施医基準と実施施設基準
植込み型VADを装着できるのは、実施医基準を満たす外科医がいる実施施設認定基準を満たした施設に限定されています。実施医基準、実施施設認定基準は「重症心不全に対する植込み型補助人工心臓治療ガイドライン」にて示されています。
INTERMACSについて
アメリカではVADの登録システムであるINTERMACSが2006年6月より開始されました。目的はVAD患者の術前リスクの層別化(重症心不全の状態を七つのカテゴリーに分類)を行い、適応の最適化を図ること、有害事象を解析して安全管理ならびに機器開発につなげることです。毎年登録データの解析結果が発表されています。
J-MACSについて *1)
日本ではINTERMACSにならって、J-MACSを2010年より開始しました。INTERMACS同様に、植込み型補助人工心臓施設認定を受けた施設が症例登録・有害事象報告を行うことが義務付けられています。
http://www.pmda.go.jp/safety/surveillance-analysis/0009.html
装着後の管理
急性期の管理
LVADの装着が必要な症例は、重症末期の心不全状態で、術前状態が不良の場合が多くみとめられ、術後の心不全管理や全身管理が非常に重要となります。特に、心不全、不整脈、神経機能障害、呼吸機能障害、高血圧症、肝機能障害、腎機能障害、感染症、出血、下肢静脈血栓塞栓症等の合併症には十分注意が必要です。
慢性期の管理
LVADの駆動状態の確認を医師、臨床工学技士が連携して毎日行う必要があります。血栓の有無や連結部の異常の有無の確認も行います。皮膚貫通部の管理は、極力消毒を行わずに洗浄中心で行います。抗凝固療法はVADが装着されている限り継続します。急性期を過ぎて、循環動態と全身状態が安定したら、リハビリテーションを開始します。
またVAD患者さんは、行動の制限や、病状、将来の移植に対する不安が加わり大きな精神的ストレスを感じています。術後早期より精神科医師、臨床心理士、看護師等と連携し患者さんと家族への精神的ケアを行う必要があります。
-
補助人工心臓(VAD)について
-
日本の補助人工心臓(VAD)治療は1980 年に三井記念病院で東大型補助人工心臓が使用されたことに始まっています。日本臨床補助人工心臓研究会の集計では、2013年8月までに1,627例が登録されています。
J-MACS *1)では平成22年(2010年)6月に患者登録を開始しました。平成26年(2014年)12月までの登録患者数424例であり、その推移は下記のとおりです。
[出典]
「日本における補助人工心臓に関連した市販後のデータ収集(J-MACS:Japanese registry for Mechanically Assisted Circulatory Support)」http://www.pmda.go.jp/safety/surveillance-analysis/0009.html
-
補助人工心臓(VAD)の役割
-
補助人工心臓(VAD)には大きく分けて下記の3つの役割があります。
- BTT (Bridge to Transplantation):心臓移植までの橋渡し
- BTR (Bridge to Recover):心臓の機能回復までの橋渡し
- DT (Destination Therapy):心不全治療としての恒久的使用
-
人工心臓の種類
-
人工心臓には完全置換型人工心臓(TAH)と補助人工心臓(VAD)があります。
TAHは自己の心臓を取り除き人工心臓に置換するものであり、循環は完全に人工心臓に依存します。
VADは自己の心臓を温存し、自己心機能と協調的に心拍出を補助します。VADは左心室の補助を行う左心室補助人工心臓(LVAD)、右心室の補助を行う右心室補助人工心臓(RVAD)、両心室の補助を行う両心室補助人工心臓(BVAD)に分類されます。また、拍動流の有無により、拍動流型人工心臓と連続流型人工心臓(無拍動流型)に分かれます。拍動流型人工心臓は生体と同じような拍動流を生み出すシステムで、より生理的であるという長所がありますが、人工弁が必要であることや装置が大型化するという欠点があります。
一方、連続流型人工心臓は、脈のない流れを生み出すシステムで、人工弁が不要であることや小型化・耐久性等の点で利点がありますが、無拍動流という非生理的な循環が生体に及ぼす影響が懸念されます。現在臨床で使用されている人工心臓は、連続流型のLVADが大半となっています。
-
適応について
-
植込み型VADの選択基準と除外基準
植込み型VADの適応は、欧米ではBTTとDTの2つに分けられますが、日本ではBTTに限定されています。植込み型VADの患者選択基準と除外基準は「重症心不全に対する植込み型補助人工心臓治療ガイドライン」にて示されています。
植込み型VADの実施医基準と実施施設基準
植込み型VADを装着できるのは、実施医基準を満たす外科医がいる実施施設認定基準を満たした施設に限定されています。実施医基準、実施施設認定基準は「重症心不全に対する植込み型補助人工心臓治療ガイドライン」にて示されています。
INTERMACSについて
アメリカではVADの登録システムであるINTERMACSが2006年6月より開始されました。目的はVAD患者の術前リスクの層別化(重症心不全の状態を七つのカテゴリーに分類)を行い、適応の最適化を図ること、有害事象を解析して安全管理ならびに機器開発につなげることです。毎年登録データの解析結果が発表されています。
J-MACSについて *1)
日本ではINTERMACSにならって、J-MACSを2010年より開始しました。INTERMACS同様に、植込み型補助人工心臓施設認定を受けた施設が症例登録・有害事象報告を行うことが義務付けられています。
http://www.pmda.go.jp/safety/surveillance-analysis/0009.html
-
装着後の管理
-
急性期の管理
LVADの装着が必要な症例は、重症末期の心不全状態で、術前状態が不良の場合が多くみとめられ、術後の心不全管理や全身管理が非常に重要となります。特に、心不全、不整脈、神経機能障害、呼吸機能障害、高血圧症、肝機能障害、腎機能障害、感染症、出血、下肢静脈血栓塞栓症等の合併症には十分注意が必要です。
慢性期の管理
LVADの駆動状態の確認を医師、臨床工学技士が連携して毎日行う必要があります。血栓の有無や連結部の異常の有無の確認も行います。皮膚貫通部の管理は、極力消毒を行わずに洗浄中心で行います。抗凝固療法はVADが装着されている限り継続します。急性期を過ぎて、循環動態と全身状態が安定したら、リハビリテーションを開始します。
またVAD患者さんは、行動の制限や、病状、将来の移植に対する不安が加わり大きな精神的ストレスを感じています。術後早期より精神科医師、臨床心理士、看護師等と連携し患者さんと家族への精神的ケアを行う必要があります。




